
近年来,伴随肿瘤靶向、免疫、核素治疗的发展,泌尿肿瘤领域取得长足进步。特别是以基因检测为代表的精准医学在泌尿肿瘤中的广泛应用,正在快速改变泌尿肿瘤领域诊疗模式。求臻医学聚焦重磅研究,紧追前沿热点,对泌尿肿瘤领域前沿进展进行梳理,特推出“探泌臻知”系列栏目。本期,我们将着重介绍保膀胱治疗相关研究进展,快跟随求小臻一起学习吧~

保膀胱治疗的临床优势

根据肿瘤的浸润深度,膀胱癌分为肌层浸润性膀胱癌(muscle-invasive bladder cancer, MIBC)和非肌层浸润性膀胱癌(non-muscle invasive bladder cancer, NMIBC)。MIBC患者的治疗方式包括:根治性膀胱切除术(RC)、膀胱部分切除术、新辅助/辅助化疗、保留膀胱综合治疗等。
根治性膀胱切除术外加盆腔淋巴结清扫术是目前治疗MIBC的标准方案。对于高危NMIBC,经尿道膀胱肿瘤电切术(transurethral resection of bladder tumor, TURBT)联合卡介苗(bacillus calmette-guerin, BCG)膀胱灌注后,若出现BCG治疗失败,也建议首选RC。但根治性膀胱切除术属于高风险手术且存在术后并发症。根据我国《膀胱癌诊疗规范(2022年版)》中的数据显示,根治性膀胱切除术的围手术期并发症可达28%-64%,再次入院率高达30%,围手术期的死亡率为2.5%-2.7%,术后总体的5年生存率约为 66%。并且根治术后的储尿和排尿问题为患者带来严重困扰,对患者的生活质量和正常社交产生极大影响。
与根治性膀胱切除术相比,保膀胱治疗可以保留膀胱的功能,避免因手术带来的不良反应和排尿方式改变,提高患者的生活质量,并且即使肿瘤复发仍然有进行挽救性手术的机会。
高危NMIBC保膀胱治疗方案及进展

不适合或拒绝膀胱根治术,及BCG灌注失败或无应答的高危NMIBC患者可以选择保膀胱治疗。最大限度经尿道膀胱肿瘤切除术(complete TURBT,cTURBT)仍是保膀胱方案的主要手术治疗措施,辅助药物治疗目前有相关临床证据的可选方案包括:(1)膀胱内灌注,常用的药物有吉西他滨、多西他赛等化疗药物;(2)免疫检查点抑制剂为基础的免疫治疗[1]。除了上述常用辅助药物治疗方案外,一些新型治疗方式也在BCG灌注失败或无应答的高危NMIBC患者中显示出较好的临床疗效。
Nadofaragene firadenovec(也称为rAd-IFNa/Syn3)是一种复制缺陷型重组腺病毒,可将人干扰素alfa-2b cDNA递送至膀胱上皮细胞,是一种用于治疗卡介苗无反应的非肌层浸润性膀胱癌的新型膀胱内疗法。一项3 期、多中心研究评估了Nadofaragene firadenovec在BCG无应答NMIBC中的疗效,103名原位癌患者中有55名(53.4%)在首次给药后3个月内完全缓解,并且这种缓解在其中25名(45.5%)患者中持续了12个月[2]。KEYNOTE-057研究在BCG治疗失败的NMIBC全身性免疫治疗探索中具有里程碑式的意义,其结果显示BCG难治性NMIBC患者接受帕博利珠单抗辅助治疗后完全缓解率可达38.8%,80%的患者完全缓解持续时间≥6个月[3]。
基于这一研究结果,另有研究探索了帕博利珠单抗+BCG膀胱灌注治疗BCG无应答NMIBC的可行性和疗效情况,结果表明6个月和1年的无复发率分别为67%(95% CI: 42-100%)和22%(95% CI: 6.5-75%),证明膀胱内帕博利珠单抗灌注治疗是安全、可行的,可以激活对BCG无应答膀胱癌的免疫反应,值得进一步研究[4]。
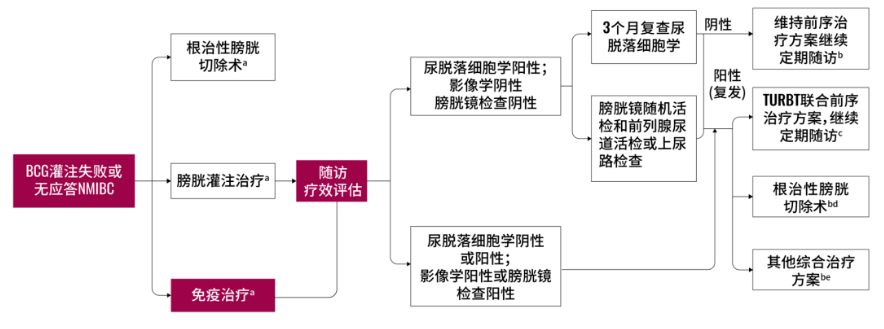
图1.NMIBC保膀胱治疗路径[1]
MIBC保膀胱综合治疗方案及进展

cTURBT和膀胱部分切除术(partial cystectomy,PC)是MIBC患者保膀胱的两种主要手术方式。对于无法通过cTURBT彻底切除的肿瘤,在特定患者中可考虑行PC[5]。下面对保膀胱综合治疗方案及进展进行详细介绍。
01 三联疗法
目前现阶段循证医学证据最充分的保膀胱综合治疗方案是三联疗法(tri-modality therapy,TMT),包含cTURBT、系统化疗以及局部放疗。奠定TMT在保膀胱治疗中地位的是RTOG(Radiation Therapy Oncology Group)系列研究(RTOG 8903、RTOG 9506、RT0G 9706、RT0G 9906、RT0G 0233)。该研究对475 名 cT2-T4a MIBC 患者进行中位时间长达7.21年的随访,发现接受TMT治疗的患者5年和10年疾病特异性生存率(disease specific survival,DSS)分别为66%和59%,5年和10年OS率分别为57%和39%,5年挽救性膀胱切除术的风险为29%[6]。
2022 ASCO-GU上,一项大型多中心匹配研究回顾性比较了834例RC患者和282例TMT患者的生存情况,结果显示,RC组和TMT组患者的5年无转移生存率为73%vs 78%(P=0.07);5年无远处转移生存率为78%vs 82%(P=0.14);5年无盆腔淋巴结转移生存率为96 vs 94%(P=0.33),均无显著差异[7]。上述研究证实了TMT的长期生存率与膀胱癌根治术相当。2022年欧洲泌尿外科学会指南推荐经过选择的患者,特别是对于不适合或不接受RC者,可选择TMT作为治疗方案[5]。
02 新型保膀胱治疗方案
近年来随着免疫治疗的加入,保膀胱综合治疗已存在越来越多的可能。
新辅助治疗转化为保膀胱治疗
临床经验和研究数据表明,通过严格的患者筛选和新辅助完成后的肿瘤综合再评估,达到cT0的患者可在保证生存的前提下,有效保留膀胱[1]。因此新辅助治疗后达到临床完全缓解(cCR)的患者或可转向保膀胱治疗。研究数据显示,26%~38%的MIBC患者会从以顺铂为基础的新辅助化疗中获得病理完全缓解(pCR),新辅助免疫单药(PURE-01、ABACUS等研究)的pCR率为29%~42%,而免疫联合化疗(BLASST-1、HCRN GU14-188、SAKK 06/17、LCCC1520和AURA等研究)的pCR率可进一步提高至34%~60%,病理降期至≤pT1期的比例达到60%~69%[5]。
一项免疫联合化疗对比单药化疗作为局部肌层浸润性尿路上皮癌新辅助治疗指导保膀胱治疗的真实世界研究显示,联合组CR率50% ,化疗组无CR;联合组和化疗组部分缓解率(PR)分别为40.9%、41.7%,疾病控制率(DCR)分别为95.4%、75%(p=0.003);联合组和化疗组一年无进展生存率(PFS)分别为95.5和62.5%(p=0.010);一年膀胱完整无病生存率(bladder-intact disease-free survival ,BI-DFS)分别为66.1%和27.5%(p=0.159),联合组肿瘤反应和肿瘤控制均显著优于化疗组[8]。免疫联合化疗的新辅助治疗方式提高了MIBC患者的pCR率,进而使得更多新辅助治疗患者可能转化为保膀胱优势患者。
TMT+免疫治疗
2021 ASCO一项多中心2期研究(NCT02621151)评估了帕博利珠单抗联合吉西他滨化疗以及同步大分割放疗作为保膀胱策略用于MIBC的效果,即在TMT基础上联合免疫治疗。研究纳入了cT2-4aN0M0的铂类不耐受或拒绝铂类化疗的MIBC患者,治疗后12周的CR率为80%,所有患者的1年预计BI-DFS为88%, 无转移生存期 (MFS)为85%[9]。
2022年ASCO-GU的NEXT研究,初步评价了局限性MIBC患者标准放化疗(CRT)后接受纳武利尤单抗辅助治疗的疗效和安全性,其6个月无失败生存率(FFS)为88.2%(95%CI:74.2%-100%),中位无复发生存期为12.2个月,这是首个关于CRT后辅助免疫治疗对局部膀胱癌作用的报告,其结果表明,辅助纳武利尤单抗具有良好的疗效[10]。
一项多中心、1b 期、开放标签、剂量递增研究确定了CRT 与三种免疫检查点抑制剂方案在非转移性 (T2-4aN0-1) MIBC 患者中的安全性,其中480 mg纳武利尤单抗单药治疗的2 年MFS为90%,3 mg/kg纳武利尤单抗联合1 mg/kg伊匹单抗治疗的1年 OS为 90%[11]。上述研究表明,在TMT方案中加入免疫治疗或将成为未来保膀胱治疗的趋势。
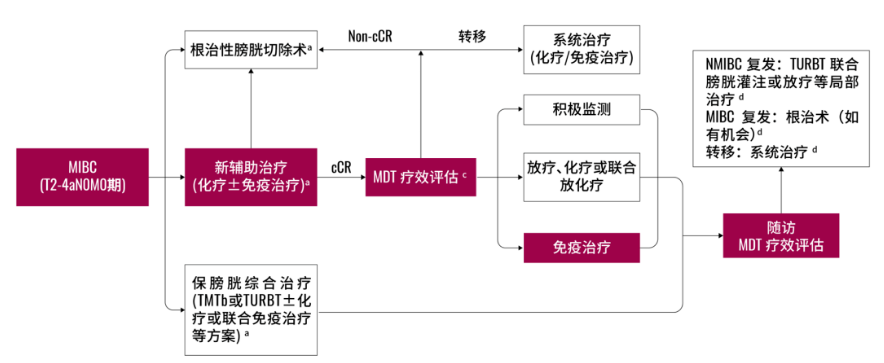
图2. MIBC保膀胱治疗路径[1]
生物标志物助力保膀胱理想人群选择

筛选适合保膀胱治疗人群能够避免治疗抵抗患者错失膀胱根治术的最佳时机,而生物标志物有望成为筛选保膀胱治疗理想人群的有效手段。有研究表明,DNA修复通路中的MRE11突变可作为放疗的不良预后因子;在接受TMT治疗的MIBC患者中,ERCC1突变与DSS的改善相关;EGFR在肌层浸润性膀胱癌中的表达与TMT治疗后预后较好相关,而HER2的过度表达则与放化疗耐药有关[12]。
另有研究发现,在TURBT+化疗(吉西他滨+顺铂)+Nivolumab治疗MIBC患者的研究中,TMB≥10mut/Mb或ERCC2突变与临床完全缓解(cCR)或病理学完全缓解(pCR)具有相关性,基因组改变或可作为预测保留膀胱无复发生存的生物标志物[13]。并且TMT后MIBC免疫浸润增加与DSS改善有关,而新辅助化疗(NAC)和根治性膀胱切除术后间质浸润增加与DSS缩短有关,因此免疫和基质特征可能是预测TMT治疗MIBC疗效的生物标志物[14]。
TRUCE-02一项替雷利珠单抗联合白蛋白紫杉醇治疗高风险NMIBC的生物标志物分析显示,AR、TCF7L2可能是预测患者不良结局的潜在标志物,而HRR突变或与较好的疗效相关[15]。上述研究表明,保膀胱治疗存在潜在疗效预测生物标志物,有望助力保膀胱理想人群选择及实现保膀胱患者的个性化精准治疗。
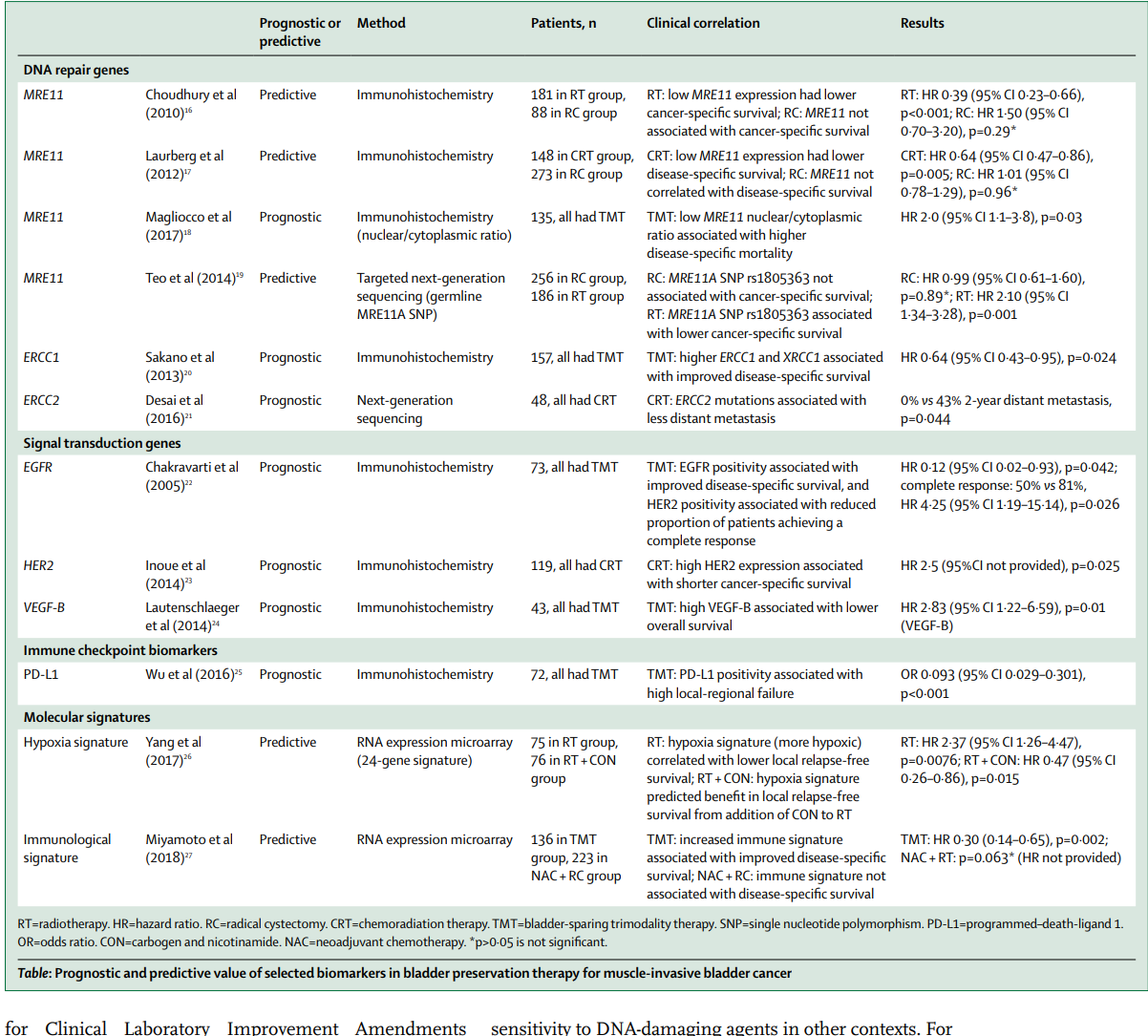
图3. MIBC中保膀胱治疗的潜在生物标志物[12]
总结

与根治性膀胱切除术相比,保膀胱治疗可以保留膀胱的功能,提高患者的生活质量。目前针对高危NMIBC及MIBC的保膀胱治疗方案越来越多,而生物标志物可筛选保膀胱理想人群,并助力选择适合的治疗方式,避免保膀胱治疗抵抗人群错失根治术的最佳时机。随着保膀胱治疗相关研究的不断推进,将有越来越多的可靠生物标志物被发现,相信在不久的未来,将有更多膀胱癌患者能够通过保膀胱治疗,实现“活着”且“活好”。



往期精选






