摘要
乳腺癌为女性第一高发恶性肿瘤,通过近年间的医学进展,部分乳腺癌患者已经可以达到接近治愈的程度,但仍有部分患者预后不良,不过临床针对这两部分人群尚不能有效提前区分,所以就会造成部分患者的治疗过度,而另一部分患者的治疗不足,导致无法治愈,进而显著地影响到其生存期及生存质量。近年间,基因检测尤其是液态活检在肿瘤领域进展迅猛,本研究发现接受新辅助治疗后仍有残留病灶的早期三阴性乳腺癌(TNBC)患者,其外周血循环肿瘤DNA(ctDNA)及循环肿瘤细胞(CTC)可以有效的区分出患者的疾病复发风险:ctDNA阳性患者肿瘤远处转移风险高接近3倍(中位DDFS,32.5个月和未达到;HR= 2.99;95%CI,1.38-6.48;P=0.006);24个月时,ctDNA阳性患者的无远处转移的可能性仅为56%,ctDNA阴性患者可达81%。本研究提示,接受新辅助治疗后仍有残留病灶的早期三阴性乳腺癌(TNBC)患者,其外周血的肿瘤相关状态对其复发、转移风险及后续治疗方案有着非常重要的参考价值。
研究背景
大部分TNBC患者需要接受新辅助化疗,其中1/3患者新辅助化疗后可获得病理完全缓解且预后良好,余下的2/3患者有残留疾病且复发风险较高。检测手术后外周循环血中的MRD可以用来确定哪些患者更可能复发,循环肿瘤DNA(ctDNA)是已建立的MRD检测方法,由于检测的是释放入循环的肿瘤组织核酸的体细胞突变,因此具有较好的特异性,即ctDNA的存在意味着疾病的存在,这项研究和其他研究证明,TNBC患者新辅助化疗和手术后血浆中检测到ctDNA提示与快速复发相关。液体活检中另一常用的分析标本是循环肿瘤细胞(CTCs),CTCs在早期和晚期乳腺癌都很常见,其计数与乳腺癌预后相关。某些情况下,即使未检测到ctDNA也可从循环中分离出CTCs,主要源于ctDNA分析可能未涵盖肿瘤特有突变或ctDNA浓度很低或很少脱落。这项研究前瞻性检测了TNBC患者新辅助化疗和手术后的ctDNA和CTCs,并着重分析了液体活检MRD与临床结果的关系。
研究方法
2014年3月26日至2018年12月18日,对BRE12-158一项II期多中心随机临床研究中196例女性患者的数据进行分析,研究中新辅助治疗后仍有残留疾病的早期TNBC患者随机分入根据基因指导的治疗或是医生选择的治疗。患者治疗分配时采集了进行ctDNA和CTCs检测的血样,142例患者进行了ctDNA与生存的分析,123例患者进行了CTCs与生存的分析。临床随访中位时间17.2个月(范围0.3-58.3个月)。主要研究终点是远处无病生存(DDFS)、无病生存(DFS)和总生存(OS)。
研究结果
196例女性患者中,检测到ctDNA的患者与较差DDFS相关(中位DDFS,32.5个月和未达到;风险比[HR] 2.99;95%CI,1.38-6.48;P=0.006)。24个月时ctDNA阳性患者的DDFS可能性为56%,ctDNA阴性患者为81%。同样,检测到ctDNA的患者与较差DFS(HR,2.67;95%CI,1.28-5.57;P=0.009)和较差OS(HR,4.16;95%CI,1.66-10.42;P=0.002)相关(图1)。ctDNA和CTCs联合可提高检测敏感性并提高鉴别能力,与ctDNA和CTCs阴性患者相比,ctDNA和CTCs阳性患者的DDFS更低(中位DDFS,32.5个月和未达到;HR,5.29;95%CI,1.50-18.62;P=0.009)。24个月时,ctDNA和CTCs阳性患者的DDFS可能性为52%,ctDNA和CTCs阴性患者为89%,DFS(HR,3.15;95%CI,1.07-9.27;P=0.04)和OS(HR,8.60;95%CI,1.78-41.47;P=0.007)也有类似趋势(图2)。


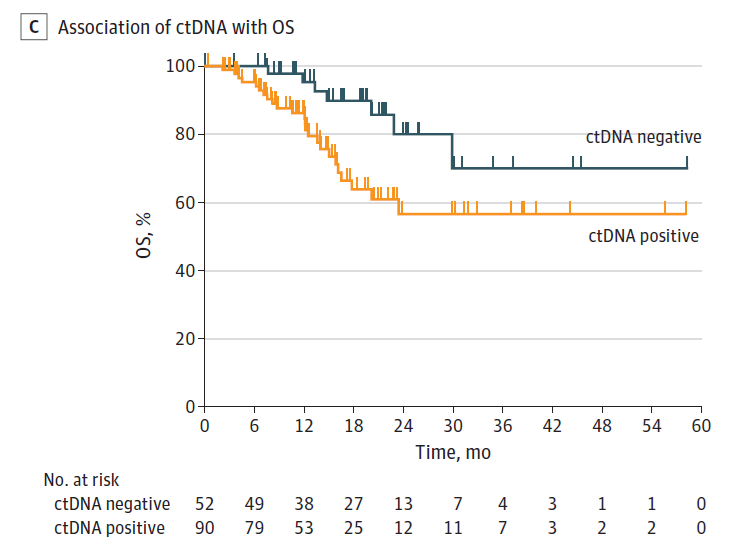
图1. 检测到和未检测到ctDNA患者的生存



图2. 检测到ctDNA和CTCs患者的生存
讨论
上述研究结果表明,新辅助治疗后未能获得完全病理缓解的TNBC患者,其高复发风险根据MRD可做进一步的风险分层,这一结果的显著性即便在考虑了多个临床变量后仍有意义,进一步支持既往研究结果,而且这项研究是迄今最大的研究之一,同时还是预先设定的前瞻性随机临床研究的二次分析结果。
对于有新辅助治疗后仍有肿瘤残留的患者,新辅助治疗后的治疗有必要加强或延长。这项研究结果支持临床研究中将MRD作为主要的分层变量,对重要基因改变进行ctDNA检测,不仅可以发现超高复发风险人群,还可以提示药物治疗靶点。同样重要的是,如果ctDNA和CTCs均阴性患者的良好结果一直能够保持,那么这些患者可能无法从额外治疗中获益,则有可能会获益于降阶治疗。上述研究结果及既往文献结果均支持常规MRD检测,可用于以治愈为目标的临床研究中的进一步风险分层。未来研究中应进一步明确分子MRD 阳性患者根据基因指导的治疗是否可进一步改善预后,这也是BRE12-158后续将进行的PERSEVERE研究的核心,即术后ctDNA阳性TNBC患者将接受与血浆测序结果相匹配的靶向药物治疗。
点评
本研究表明,不是所有新辅助化疗后有疾病残留的TNBC均有高危转移风险,ctDNA有望成为新辅助化疗后的进一步风险分层的重要参考指标,并可进一步获益于与之相匹配的靶向治疗,进而使得这部分高风险患者的生存期及生活质量得以进一步显著延长。
ChosenOne599®基于液态活检(ctDNA样本)的测序深度达到30000x,可准确识别低至0.1% 的乳腺癌驱动基因突变,以辅助围术期药物治疗决策;在此基础上,ChosenOne599®提示ctDNA状态(阴性/阳性),为乳腺癌术后复发风险分层提供更多参考信息。
参考文献:
Association of Circulating Tumor DNA and Circulating Tumor Cells After Neoadjuvant Chemotherapy With Disease Recurrence in Patients With Triple-Negative Breast Cancer. JAMA Oncol. 2020






