同源重组缺陷(HRD)
DNA在细胞内外因素的影响下发生碱基错配、链断裂等损伤时,DNA损伤修复系统可以自发修复损伤的DNA,从而避免出现过多的有害变异。肿瘤细胞和正常细胞均会使用这些修复途径。

图1. DNA损伤修复
DNA损伤反应(DDR)是细胞对外源性和内源性基因毒性损伤的反应,可产生DNA单链断裂(SSB)和DNA双链断裂(DSB)。单链断裂可通过核苷酸切除修复(NER)、碱基切除修复(BER)或错配修复(MMR),双链断裂修复是通过同源重组(HR)机制。单链断裂(SSB)主要由PARP参与修复;双链断裂修复主要由BRCA1/2参与的同源重组修复(HRR)。除了BRCA1和BRCA2,其它HRR相关基因,如PALB2, CDK12,RAD51, CHEK2, ATM等发生突变都会引起同源重组缺陷(HRD),导致基因组不稳定。
02
PARP抑制剂(PARPi)
PARP酶是存在于多数真核细胞中的一个多功能蛋白酶,PARP酶全名为多腺苷二磷酸核糖聚合酶(poly ADP ribose polymerase,PARP)。PARP酶作为DNA修复酶,负责DNA断裂单链的修复。抑制PARP酶的靶向药物即是PARP抑制剂,PARP抑制剂对PARP的作用机制包括2个方面 :①在PARP活性位点与烟酰胺腺嘌呤二核苷酸竞争,抑制多聚(ADP-核糖)聚合物形成 ;②结合到PARP的结合口袋中,造成构象变化,使PARP保持对DNA的结合,从而使DNA-PARP复合物长期存在,抑制DNA后续修复过程。

图2. PARP酶修复DNA单链断裂
03
PARP抑制剂的“合成致死”效应
PARP在DNA单链碱基切除、修复过程中发挥关键作用,如果使用PARP抑制剂阻断单链修复,在同源重组缺陷(HRD)的肿瘤细胞中,肿瘤细胞DNA得不到修复,将会形成“合成致死”效应,导致肿瘤细胞死亡;正常细胞同源重组修复基因后继续生存,不会被PARP抑制剂杀死。

图3.PARP抑制剂的“合成致死”效应
目前美国FDA和中国NMPA批准了多款PARP抑制剂用于临床(如图4所示),BRCA基因突变或HRD是目前常用的PARP抑制剂生物标志物。
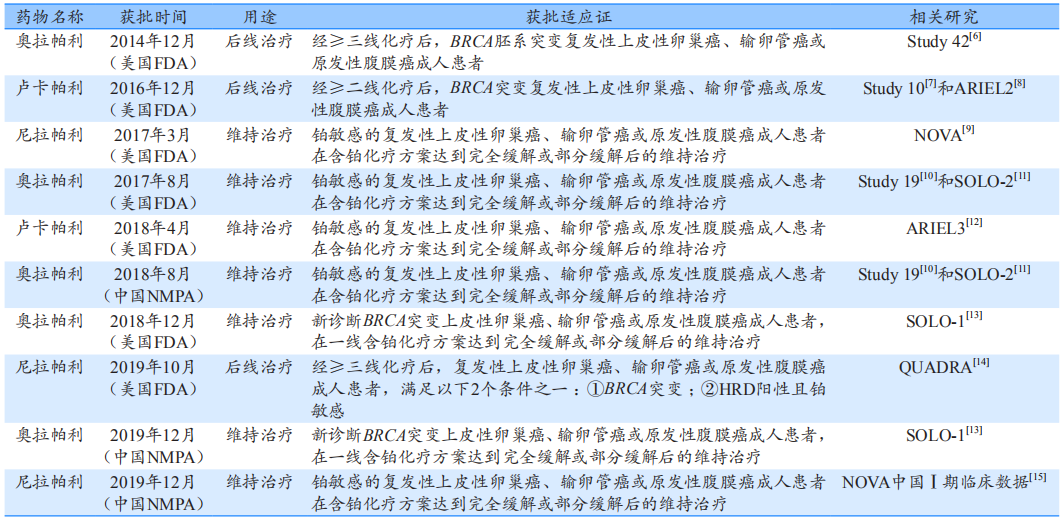
图4. PARP抑制剂在美国FDA或中国NMPA获批适应证
04
HRD是独立预测奥拉帕利维持治疗的指标
尽管BRCA1/2基因突变是首选的PARP抑制剂敏感生物标志物,除BRCA基因突变外,其他HRR基因,如RAD51、ATM、PALB2、MRE11等损伤或缺失也会导致HRD,因此HRD作为PARP抑制剂敏感的生物标志物已应用于临床。PAOLA-1研究纳入新确诊的Ⅲ-Ⅳ期高级别浆液性或子宫内膜样卵巢癌、输卵管癌及原发性腹膜癌患者,对照组使用贝伐珠单抗联合安慰剂进行维持治疗,实验组使用贝伐珠单抗联合奥拉帕利治疗。HRD阳性(包含BRCA突变)患者两组的中位PFS分别为37.2个月和17.7个月(HR =0.33);HRD阳性(排除BRCA突变)患者两组的中位PFS分别为28.1个月和16.6个月(HR= 0.43);HRD阴性/未知患者两组的中位PFS分别为16.9个月和16.0个月(HR=0.92)。HRD阳性患者(无论是否包含BRCA突变)接受奥拉帕利治疗的中位PFS远高于对照组,HRD是独立于BRCA突变预测奥拉帕利维持治疗疗效的指标。

图5. PAOLA-1研究显示HRD阳性患者有更长的PFS
除PAOLA-1研究外,在其他几项卵巢癌PARP抑制剂相关的临床研究中,HRD检测阳性的患者对铂类药物以及PARP抑制剂高度敏感也同样得到了证实(如图6和图7)。

图6.HRD检测与卵巢癌PARP抑制剂一线维持治疗
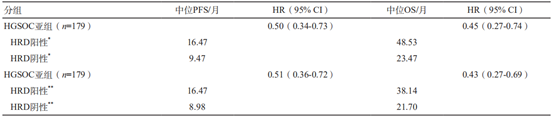
图7.HRD检测与卵巢癌的铂类药物化疗
05
HRD检测方法
HRD主要病因有3种:①突变(包括胚系BRCA基因、胚系HR基因和体细胞HR基因),②结构重排(LOH,杂合性丢失;TAI,端粒等位基因失平衡;LST,大片段迁移),③表观遗传修饰(启动子甲基化)。

图8.HRD病因
针对突变,目前NGS测序既可检测出,通常在多基因Panel上进行。HR基因突变同样分为胚系变异和体细胞变异,解读原则与BRCA1/2相同。针对结构重排,NGS检测后进行基因组不稳定性状态的评分(HRD score),由LOH、TAI、LST三项综合计算得出。
求臻医学大Panel产品上线HRD算法,基于中国人群数据研发,制定了更适用于中国患者的评分系统,助力肿瘤患者尤其是BRCA阴性的患者,全面从PARP抑制剂中获益。
求臻医学大Panel产品除了BRCA1/2基因以外,还包含ATM、BARD1、BRIP1、CDK12、CHEK1、CHEK2、FAM175A、FANCA、MRE11A、NBN、PALB2、RAD51C、RAD51D、RAD54L等有相对明确的临床数据支持的、与PARP抑制剂疗效相关的部分HRR基因。
检测内容
一、HRD-Score:综合LOH(染色体杂合性缺失)、LST(大片段迁移)、TAI(端粒等位基因失衡)三个指标进行基因组不稳定性评分。
二、HRR基因胚系突变+体系突变。
临床意义
HRD检测越来越多的被推荐用于指导卵巢癌患者治疗方案的选择,HRD检测阳性的患者对铂类药物以及PARP抑制剂高度敏感。对于没有BRCA突变的患者,HRD检测阳性的患者可以获得PARP抑制剂治疗获益信息,同时卵巢癌中HRD阳性人群占比接近50%,相对于占比不到20% BRCA突变患者,HRD检测将扩大靶向治疗的获益人群,为更多患者争取靶向治疗的机会。
适用人群
1. 新诊断或复发性的卵巢癌、输卵管癌、原发性腹膜癌成人患者
2. HER2阴性的局部晚期或转移性乳腺癌患者
3. 转移性去势抵抗前列腺癌患者
4. 转移性胰腺癌患者
5. BRCA1/2阴性的卵巢癌、乳腺癌、前列腺癌、胰腺癌患者
6. 拟尝试PARP抑制剂异病同治的其他肿瘤患者
7. 有乳腺癌、卵巢癌、结直肠癌等HRD高风险家族性肿瘤的健康人群
注:目前HRD评分正在进行中国人群的临床试验,因此阳性阈值仅供参考。
参考文献:
1. Use of poly ADP-ribose polymerase [PARP] inhibitors in cancer cells bearing DDR defects: the rationale for their inclusion in the clinic
2. Targeted treatment of advanced ovarian cancer: spotlight on rucaparib
3. 卵巢癌PARP抑制剂临床应用指南
4. Investor science conference call:European Society for Medical Oncology (ESMO) Congress 2019
5. 上皮性卵巢癌PARP抑制剂相关生物标志物检测的中国专家共识
6. Homologous Recombination Deficiency in Breast Cancer: implications for risk, cancer development and therapy






